ВИЧ-инфекция - хроническая инфекционная болезнь, вызванная ВИЧ (human immunodeficiency virus infection - HIV-infection). ВИЧ-инфекция - медленно прогрессирующее антропонозное заболевание с контактным механизмом передачи возбудителя, характеризующееся поражением иммунной системы с развитием СПИДа. Клинические проявления СПИДа, приводящие к гибели инфицированного человека, - оппортунистические (вторичные) инфекции, злокачественные новообразования и аутоиммунные процессы.
КОДЫ ПО МКБ-10
B20 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде инфекционных и паразитарных болезней.
B21 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде злокачественных новообразований.
B22 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других уточненных болезней.
B23 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), проявляющаяся в виде других состояний.
B24 Болезнь, вызванная вирусом иммунодефицита человека (ВИЧ), неуточненная.
Z21 Бессимптомный инфекционный статус, вызванный вирусом иммунодефицита человека (ВИЧ).
ЭТИОЛОГИЯ
Возбудитель
Описано два типа - ВИЧ-1 и ВИЧ-2, различающиеся по структурным и антигенным характеристикам. На территории Российской Федерации эпидемиологическое значение имеет ВИЧ-1 (основной возбудитель заболевания).
Систематика ВИЧ
ВИЧ относят к царству Viridae семейству Retroviridae роду Lentiviridae.
ОСНОВНЫЕ СВОЙСТВА ВИРУСА ИММУНОДЕФИЦИТА ЧЕЛОВЕКА
Строение вирусной частицы
Вирус имеет округлую форму и сложную структуру. Диаметр вириона составляет 100120 нм. Специфические белки вируса представлены в таблице (табл. 21.8).
Таблица 21.8. Группы белков ВИЧ-1 и ВИЧ-2
|
Группы белков |
ВИЧ-1 |
ВИЧ-2 |
|
Белки оболочки вируса (env) |
gp160, gp120, gp41 |
gp140, gp105,gp36 |
|
Белки сердцевины(дад) |
p17, p24, p55 |
p16, p25, p56 |
|
Ферменты вируса (pol) |
p31, p51, p66 |
p68 |
* Молекулярный вес белков измеряют в килодальтонах (кДа); gp - гликопротеины; р - протеины.
В центре вириона располагается геном вируса, представленный двумя нитями РНК, внутренними протеинами p7 и p9, а также ферментами - обратной транскриптазой (ревертазой), протеазой, РНКазой и интегразой (эндонуклеазой). Геном окружает внутренняя белковая оболочка. В состав внутренней оболочки ВИЧ-1 входят протеины p17, p24 и p55. Протеины p16, p25 и p56 образуют внутреннюю оболочку ВИЧ-2. Наружная липидная оболочка ВИЧ-1 пронизана гликопротеином gp160, состоящим из трансмембранного (gp41) и высокоиммуно-генного (gp120) фрагмента. Оболочечные белки gр41 и gр120 соединены нековалентной связью и формируют на поверхности вириона отростки, обеспечивающие присоединение ВИЧ к рецепторам клеток-мишеней человека. Геном вируса содержит 9 генов - три структурных и шесть регуляторных. Геном является изменчивой структурой за счет антигенного дрейфа.
Существует ряд вариантов вируса [основная группа М, состоящая из нескольких подтипов (клад): А, В, С, D, Е, F, G, Н, I, J, K; группы O, N, P].
Устойчивость вируса в окружающей среде
В естественных условиях ВИЧ (в высушенном состоянии) сохраняет активность в течение нескольких часов; в жидкостях, содержащих большое количество вирусных частиц, таких, как кровь и эякулят, - в течение нескольких дней.
В замороженной сыворотке крови активность вируса определяют на протяжении нескольких лет.
Нагревание до 56 °С в течение 30 мин приводит к снижению инфекционного титра вируса в 100 раз. При более высокой температуре (70-80 °С) вирус погибает через 10 мин. Вирус чувствителен к 70% раствору этанола (Этиловый спирт*), 0,5% раствору гипохлорита натрия, 1% раствору глутаральдегида, 6% раствору водорода пероксида, 5% раствору лизола, эфира или ацетона.
ВИЧ относительно мало чувствителен к ультрафиолетовому облучению и ионизирующей радиации.
ЭПИДЕМИОЛОГИЯ
Источник (резервуар) вируса иммунодефицита человека
Источник ВИЧ-инфекции - ВИЧ-инфицированные люди, находящиеся на любой стадии заболевания, независимо от наличия или отсутствия клинических проявлений болезни, в том числе в периоде инкубации.
Механизмы, пути и факторы передачи
Основной механизм передачи инфекции - контактный. Существуют естественные и искусственные пути передачи. К естественным путям передачи относят половой (при половых контактах) и вертикальный (от инфицированной матери ребенку в период беременности, родов или при грудном вскармливании).
Искусственный (артифициальный) путь передачи - парентеральный - реализуется при проникновении вируса в кровь при различных манипуляциях, связанных с нарушением целостности слизистых оболочек и кожных покровов.
К числу факторов, влияющих на вероятность инфицирования полового партнера ВИЧ, относят титр вируса у источника инфекции; наличие у реципиента различных заболеваний половых органов; интенсивность контакта.
Современная эпидемиология ВИЧ-инфекции исключает существование аэрозольного, фекально-орального и трансмиссивного механизмов передачи вируса.
Восприимчивость человека к ВИЧ практически стопроцентная. Фактором невосприимчивости к заражению ВИЧ может быть отсутствие определенных специфических рецепторов. В настоящее время выделяют гены, контролирующие синтез молекул, участвующих в проникновении ВИЧ в клетки хозяина. Таким образом, люди, имеющие гомозиготный генотип по этим генам, устойчивы к заражению ВИЧ половым путем; лица с гетерозиготным генотипом - менее устойчивы. Было установлено, что длительно контактирующие с ВИЧ-инфицированными и при этом не заразившиеся люди имеют генетический вариант CCR5-32, представляющий собой мутацию в гене, отвечающем за экспрессию корецептора CCR5 на поверхности лимфоцитов. Однако этот признак не ассоциируют с невосприимчивостью к ВИЧ при переливании крови или при внутривенном введении психоактивных веществ.
ВИЧ-инфекция распространена повсеместно. Вместе с тем распространенность ВИЧ- инфекции крайне неравномерна в различных регионах, разных возрастных, социальных и профессиональных группах. Наибольшее количество ВИЧ-инфицированных проживают в Центральной Африке (к югу от пустыни Сахары) и на Карибских островах. Важным показателем считают прирост числа новых случаев. В начале 80-х гг. ХХ в. максимальное количество случаев ВИЧ-инфекции регистрировали в Центральной Африке и в США, а к концу 2000 г. в эпидемию были вовлечены уже все континенты. В России ВИЧ-инфекцию регистрируют с 1985 г., первоначально среди иностранцев, преимущественно выходцев из Африки, а с 1987 г. - среди граждан СССР. С 2006 г. ВИЧ-инфекцию обнаруживают и регистрируют во всех субъектах РФ.
До середины 90-х гг. ХХ в. в РФ основным путем передачи ВИЧ считали половой. Это определяло своеобразие эпидемического процесса инфекции. Со второй половины 1996 г. произошла смена ведущего пути передачи инфекции. Первое место заняло «инъекционное» заражение, как правило, среди наркоманов, практикующих парентеральное введение психоактивных веществ. В последние годы увеличивается значимость гетеросексуального пути передачи ВИЧ-инфекции. Об этом свидетельствует не только увеличение количества инфицированных (основной фактор риска для которых - гетеросексуальные контакты), но и рост доли инфицированных женщин. Вследствие этого повышается вероятность передачи ВИЧ- инфекции от матери к ребенку.
МЕРЫ ПРОФИЛАКТИКИ
Знание эпидемиологических и клинических особенностей ВИЧ-инфекции позволило разработать комплекс профилактических и противоэпидемических мероприятий. Профилактика только неспецифическая. Попытки создать вакцину до настоящего времени успеха не имели.
Неспецифическая профилактика
Неспецифическая профилактика заключается в предотвращении половой и перинатальной передачи ВИЧ; в контроле безопасности переливаемых компонентов крови и ее препаратов, а также в предупреждении передачи инфекции при проведении медицинских манипуляций. Большое значение имеет также оказание специфической специализированной медицинской помощи.
ПАТОГЕНЕЗ
Дифференцировочный антиген CD4+ (CD - аббревиатура от Cell Differention antigen) и неспецифические (независящие от наличия CD4+) компоненты - рецепторы для ВИЧ. CD4+ - гликопротеид с молекулярной массой 55 000 кД, по своему строению схожий с определенными участками Ig. Аналогичное строение имеет и белок вируса gp120; это и определяет способность проникновения вирионов в клетку.
Рецептор CD4+, расположенный на мембране иммунокомпетентных клеток, выполняет функцию распознавания антигенов (вместе с белками HLA - главного комплекса гистосовместимости II класса).
В организме человека существует целый ряд иммунокомпетентных, соматических и других клеток, несущих рецепторы для ВИЧ (табл. 21.9).
Таблица 21.9. Типы клеток, поражаемых вирусом иммунодефицита человека
|
Тип клеток |
Ткани и органы |
|
Т-лимфоциты, макрофаги |
Кровь |
|
Клетки Лангерганса |
Кожа |
|
Фолликулярные дендритные клетки |
ЛУ |
|
Альвеолярные макрофаги |
Легкие |
|
Эпителиальные клетки |
Толстый кишечник, почки |
|
Клетки шейки матки |
Шейка матки |
|
Клетки олигодендроглии |
Головной мозг |
Оболочка ВИЧ содержит белки человеческого комплекса гистосовместимости I и II классов, поэтому проникновение вируса в организм не вызывает реакции отторжения. Фиксация вирионов на поверхности клетки-мишени происходит при участии гликопротеина gp120. Гликопротеин gp41 обеспечивает слияние вирусной оболочки с мембраной клетки-мишени. Двухцепочечная РНК вируса проникает в клетку, где с помощью обратной транскриптазы происходит синтез одноцепочечной провирусной ДНК. Затем происходит формирование двухце-почечной ДНК, встраивающейся в ДНК клетки с помощью интегразы. Вирусная ДНК выполняет функцию матрицы для синтеза РНК, собирающей новую вирусную частицу.
Нередко при репликации ВИЧ возникают генетические ошибки. Таким образом происходит образование разных подтипов вируса.
После проникновения ВИЧ в СD4+-клетки начинается его репликация: чем активнее СD4+-клетки, тем интенсивнее репродукция вируса. Поэтому регуляторы, активирующие СD4+-клетки, обеспечивают увеличение репликации вируса.
К подобным регуляторам относят ФНО; фактор, стимулирующий колонии гранулоцитов и макрофагов (колониестимулирующий фактор) и ИЛ-6.
ИФН и трансформирующий фактор роста - регуляторы, тормозящие репликацию вируса. Как показали исследования, ФНО-а активирует транскрипцию провирусной ДНК ВИЧ-1 в хронически инфицированных Т-клетках и макрофагах. Моноциты, синтезирующие ФНО-а, не только индуцируют экспрессию ВИЧ-инфицированными клетками, но и стимулируют активацию латентного провируса. Регистрируют одновременную активность ФНО-а, ИЛ-6 и фактора, стимулирующего колонии гранулоцитов и макрофагов.
Иммунопатогенетические признаки ВИЧ-инфекции - дефицит Т-звена и В-звена иммунной системы; недостаток компонентов комплемента и фагоцитов; снижение функций неспецифических факторов защиты. Поликлональная активация В- лимфоцитов приводит, с одной стороны, к гипергаммаглобулинемии, а с другой - к ослаблению способности клеток продуцировать вируснейтрализующие антитела. Происходит увеличение количества ЦИК и образование антител к лимфоцитам; это вызывает еще большее уменьшение числа CD4+-Т-лимфоцитов. Отмечают развитие аутоиммунных процессов. Поражение иммунной системы при ВИЧ-инфекции носит системный характер.
Наряду с дефицитом CD4+-лимфоцитов в течение болезни нарастает функциональная недостаточность CD8+-лимфоцитов, NK-клеток (естественных киллеров) и нейтрофилов. При ухудшении иммунного статуса развиваются различные инфекционные, аллергические, аутоиммунные и лимфопролиферативные заболевания, а также синдром, свойственный болезни иммунных комплексов (эти факторы определяют клиническую картину ВИЧ-инфекции).
На начальных стадиях заболевания в организме вырабатываются вируснейтрализующие антитела, подавляющие активность свободно циркулирующих вирусов. Однако такие антитела не действуют на вирусы, находящиеся в клетках (провирусы). С течением времени (обычно после 5-6 лет) происходит истощение защитных возможностей иммунной системы и, следовательно, накопление вируса в крови.
КЛИНИЧЕСКАЯ КАРТИНА
Продолжительность инкубационного периода ВИЧ-инфекции составляет от 2 нед до 6 мес и более.
Период первичных клинических проявлений (острая стадия)
Острая стадия ВИЧ-инфекции может протекать скрыто или сопровождаться множественными неспецифическими симптомами. В 50-70% случаев наступает период первичных клинических проявлений, при этом отмечают лихорадку, ЛАП, эритематозную или макулопапулезную сыпь на лице, туловище и конечностях; миалгии или артралгии. Реже больные жалуются на диарею, головную боль, тошноту, рвоту. Возможно увеличение печени и селезенки. Неврологические симптомы - менингоэнцефалит или серозный менингит - обнаруживают примерно у 12% больных. Длительность острой стадии инфекции - от нескольких дней до 2 мес. Как правило, из-за сходства признаков острой стадии с симптомами гриппа и других распространенных заболеваний распознать ВИЧ-инфекцию на данном этапе сложно. Кроме того, часто период острой стадии протекает бессимптомно. В течение данного периода подтвердить диагноз можно только при помощи ПЦР. ПЦР позволяет обнаружить РНК вируса. Иногда определяют протеин p24 - антиген ВИЧ.
Антитела к ВИЧ в период острой стадии, как правило, не обнаруживают. В первые 3 мес после заражения антитела к ВИЧ появляются у 90-95% пациентов, через 6 мес - у остальных 5-9%, а в более поздние сроки - только у 0,5-1%. В стадии СПИДа регистрируют существенное снижение содержания антител в крови.
Бессимптомный период
Следующий период ВИЧ-инфекции - бессимптомный, продолжающийся несколько лет - пациенты чувствуют себя удовлетворительно и ведут обычный образ жизни.
Генерализованная лимфаденопатия
После острой инфекции возможно развитие персистирующей генерализованной ЛАП. В исключительных случаях болезнь может сразу прогрессировать вплоть до терминальной стадии (СПИД).
При персистирующей генерализованной ЛАП отмечают увеличение как минимум двух групп ЛУ (от 1 см и более у взрослых, за исключением паховых ЛУ, и от 0,5 см - у детей), сохраняющееся не менее 3 мес. Наиболее часто увеличиваются шейные, затылочные и подмышечные ЛУ.
Продолжительность стадии персистирующей генерализованной ЛАП составляет 5-8 лет. В течение всего периода регистрируют периодические уменьшение и увеличение ЛУ. В стадию ЛАП отмечают постепенное снижение уровня CD4+-лимфоцитов. Пациентов, страдающих бессимптомной инфекцией или персистирующей генерализованной ЛАП, выявляют при случайном обследовании (как правило, больные активно к врачу не обращаются).
Общая продолжительность инкубационного и бессимптомного периодов варьирует от 2 до 10-15 лет (в отдельных случаях и более).
Период вторичных клинических проявлений
За бессимптомным периодом следует симптоматическая хроническая фаза ВИЧ- инфекции, характеризующаяся развитием различных заболеваний вирусной, бактериальной, грибковой и протозойной природы, нередко протекающих благоприятно при традиционных методах лечения. Как правило, регистрируют повторные заболевания (отиты, синуситы и трахеобронхиты, тонзиллиты); поверхностные поражения кожи, слизистых оболочек (локализованная форма рецидивирующего простого герпеса, рецидивирующий опоясывающий герпес, кандидоз слизистых оболочек, дерматомикозы и себорея).
С течением времени такие инфекции приобретают затяжной характер и устойчивость к стандартным методам лечения, что обусловливает развитие более серьезных осложнений. Пациента могут беспокоить лихорадка, повышенная ночная потливость, диарея, потеря веса.
На фоне нарастающей иммуносупрессии развиваются тяжелые прогрессирующие заболевания, которые обычно не встречаются у людей с нормально функционирующей иммунной системой. Такие состояния называют СПИД- индикаторными.
Классификация
Согласно принятой в Российской Федерации классификации (приказ Минздравсоцразвития РФ от 17 марта 2006 г. № 166), выделяют следующие стадии ВИЧ-инфекции.
1. Инкубации.
2. Первичных проявлений, в которой выделяют:
A. бессимптомную ВИЧ-инфекцию;
Б. острую ВИЧ-инфекцию без вторичных заболеваний;
B. острую ВИЧ-инфекцию с вторичными заболеваниями.
3. Латентная (субклиническая).
4. Вторичных заболеваний.
A. Потеря массы тела менее 10%; грибковые, вирусные, бактериальные поражения кожи и слизистых оболочек; повторные фарингиты и синуситы; опоясывающий герпес. Фазы:
прогрессирование:
- при отсутствии АРВТ;
- на фоне АРВТ; ремиссия:
- спонтанная;
- после ранее проводимой АРВТ;
- на фоне АРВТ.
Б. Потеря массы тела более 10%; необъяснимая диарея или лихорадка более 1 мес; волосатая лейкоплакия; туберкулез легких; стойкие повторные вирусные, бактериальные, грибковые, протозойные поражения внутренних органов; локализованная саркома Капоши; повторный или диссеминированный опоясывающий герпес. Фазы: прогрессирование:
- при отсутствии АРВТ;
- на фоне АРВТ; ремиссия:
- спонтанная;
- после ранее проводимой АРВТ;
- на фоне АРВТ.
B. Кахексия; генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания, в том числе кандидоз пищевода, бронхов, трахеи, легких; пневмоцистная пневмония; внелегочный туберкулез; диссеминированная саркома Капоши; атипичные микобактериозы; злокачественные опухоли; поражения ЦНС различной этиологии.
Фазы:
прогрессирование:
- при отсутствии АРВТ;
- на фоне АРВТ; ремиссия:
- спонтанная;
- после ранее проводимой АРВТ;
- на фоне АРВТ.
5. Терминальная.
Основные симптомы ВИЧ-инфекции и динамика их развития
Стадия первичных клинических проявлений начинается с периода сероконверсии [иногда в самом начале диагностируют острую (лихорадочную) стадию]. Стадия 2 наблюдается у 50-70% пациентов и нередко предшествует наступлению сероконверсии. Клинические признаки острой стадии (часто имеют неспецифический характер) - выраженная интоксикация, слабость, лихорадка, лимфаденопатия, эритематозно-макулезная сыпь, боли в мышцах и суставах, катаральные явления (иногда в сочетании с сыпью на коже), увеличение печени и селезенки: тонзиллит, полиаденит. Возможны преходящие нарушения деятельности ЦНС (от головных болей до острой обратимой энцефалопатии с потерей ориентации, памяти и нарушениями сознания, серозного менингита или менингоэнцефали-та). В сыворотке крови обнаруживают антитела к ВИЧ (не постоянно). Нередко антитела к ВИЧ выявляют в конце острой стадии. Острая стадия развивается не у всех пациентов, а вследствие трудности ее диагностики число таких случаев оценить сложно. Манифестное течение периода острой сероконверсии при ВИЧ-инфекции - неблагоприятный признак быстрого прогрессирования заболевания.
Продолжительность лихорадочного состояния - от 1-2 нед до 1 мес. Подтвердить диагноз можно путем обнаружения методом ПЦР РНК ВИЧ, иногда определяется антиген ВИЧ - протеин р24.
Субклиническая стадия 3 наступает либо сразу после острой стадии, либо начинает стадию первичных проявлений. Этот период характеризуют положительные серологические реакции на ВИЧ при проведении ИФА и иммунного блоттинга (ИБ) при отсутствии клинических признаков заболевания. Длительность субклинической стадии варьирует от 2-3 мес до нескольких лет.
В бессимптомную стадию возможно развитие персистирующей генерализованной ЛАП (в среднем продолжительность инфекционного процесса составляет от 6 мес до 5 лет). В данный период единственный клинический симптом заболевания - генерализованная ЛАП - увеличение ЛУ (не менее 1 см в диаметре) в двух или более несоприкасающихся внепаховых локусах, сохраняющее свой объем в течение по меньшей мере 3 мес при отсутствии какого-либо текущего заболевания. Помимо генерализованной ЛАП, наблюдают увеличение печени, селезенки; астенический синдром. Наблюдается постепенное снижение уровня CD4+-лимфоцитов. Общая продолжительность инкубационного и бессимптомного периодов от 2 до 10-15 лет и более.
Стадию вторичных заболеваний характеризуют развивающиеся на фоне иммунодефицита бактериальные, вирусные, грибковые, протозойные инфекции или опухолевые процессы. Стадию 4А рассматривают как переходный период от персистирующей генерализованной ЛАП к СПИД-ассоциированному комплексу. При этом длительность инфекционного процесса составляет 3-7 лет и более. Отмечают более выраженный астенический синдром, снижение умственной и физической работоспособности, ночную потливость, периодические подъемы температуры до субфебрильных цифр, неустойчивый стул, потерю массы тела менее 10%. Эта стадия заболевания протекает без выраженных оппортунистических инфекций и инвазий, а также без развития саркомы Капоши и других злокачественных опухолей. Возможны различные заболевания кожи (иногда это обострившиеся прежние, но чаще - приобретенные), обусловленные грибковым, вирусным, бактериальным или другим поражением - себорейный или аллергический дерматит, псориаз, папулезная сыпь. Грибковое поражение кожи приводит к развитию онихомикоза, дерматомикоза стоп (кистей, голеней и других участков тела). Вирусные поражения - простой герпес, опоясывающий герпес, остроконечные кондиломы, контагиозный моллюск, бородавки. Стафилококковые и стрептококковые фолликулиты, импетиго и эктима - признаки бактериальных инфекций. На слизистых оболочках обнаруживают афты; развивается ангулярный хейлит, гингивит. Нередко развиваются рецидивирующие инфекции верхних дыхательных путей, включая бактериальные синуситы.
Признаки прогрессирования заболевания (стадия 4Б) - общие симптомы без генерализации оппортунистических инфекций или опухолей, появляющиеся в более поздние стадии заболевания. Характерны необъяснимые длительная лихорадка перемежающегося или постоянного типа и хроническая диарея (длительность симптомов - всегда больше месяца), потеря более 10% массы тела. Могут иметь место поражения кожи и слизистых оболочек грибковой (орофа-рингеальный кандидоз, реже - генитальной и перианальной областей), вирусной (волосатая лейкоплакия, повторный или рецидивирующий Herpes Zoster), телеангиэктазии, геморрагические высыпания, лейкопластический васкулит, гиперальгезивный псевдотромбофлебитический синдром и локализованная форма саркомы Капоши. При бактериальных поражениях кожи и слизистых оболочек возможно развитие вегетирующей, шанкриформной и диффузной форм хронической пиодермии, целлюлита, пиомиозита, пиогенных гранулем, фурункулов и абсцессов. Выявляют бактериальные (в том числе легочный туберкулез), вирусные, грибковые и протозойные поражения внутренних органов (без диссеминации).
Наблюдается тенденция к анемии, тромбоцитопении и лейкопении, обусловленной главным образом лимфопенией и лишь в незначительной степени - ней-тропенией. Вирус активно размножается и оказывает супрессорное воздействие на иммунную систему; нарастают признаки иммунодефицита. Определяют уменьшение количества CD4+-лимфоцитов до 200-300 мкл-1, CD8+-лимфоцитов - до 1300 мкл-1; при этом соотношение количества CD4+/CD8+-лимфоцитов снижается до 0,5.
Стадия 4В соответствует развернутому СПИДу. Как правило, симптомы данной стадии обнаруживают при длительно текущем инфекционном процессе (более 5 лет). Нарастающий иммунодефицит приводит к развитию двух основных клинических проявлений СПИДа: оппортунистические инфекции, вызванные условно-патогенной флорой, и новообразования. Любые патогенные микроорганизмы вызывают необычно тяжелое течение соответствующей инфекции.
Клинические состояния, возникающие на стадии 4В
Основные протозойные инфекции - токсоплазмоз головного мозга, протекающий в форме энцефалита, и криптоспоридиоз, характеризующийся длительной (более месяца) диареей. Наблюдаются случаи изоспоридиоза, микроспоридиоза, висцерального лейшманиоза, лямблиоза и амебиаза.
Группу грибковых инфекций составляют кандидоз пищевода и трахеи, бронхов и легких, пневмония, вызванная P. jirovecii; экстрапульмональный криптококкоз (протекает, как правило, в форме менингита) или менингоэнцефалита. Нередко развиваются диссеминированные эндемичные микозы - гистоплазмоз, кокци-диоидоз и аспергиллез.
Основные вирусные заболевания - инфекции, вызванные ВПГ. ВПГ приводит к развитию длительно (более месяца) сохраняющихся признаков поражения кожи и слизистых оболочек; а также обусловливает возникновение генерализованной формы инфекции (любой продолжительности) с вовлечением в патологический процесс бронхов, легких, пищевода и нервной системы. У ВИЧ-инфицированных пациентов диагностируют ЦМВИ не только печени, селезенки и ЛУ, но и других органов (как правило, развивается генерализованная форма заболевания, с поражением сетчатой оболочки глаз, ЦНС, легких, пищевода и толстой кишки). Реже обнаруживают диссеминированный опоясывающий герпес, прогрессирующую мультифокальную лейкоэнцефалопатию (паповавирус), инфекцию, вызванную ЭБВ.
Наиболее часто развивающиеся бактериальные инфекции - атипичный диссеминированный микобактериоз с поражением легких, кожи, периферических ЛУ, ЖКТ, ЦНС и других органов; внелегочный туберкулез; нетифоидная сальмо- неллезная септицемия. Реже диагностируют стафилококковую и стрептококковую бактериемию, а также легионеллез.
Индикаторные опухолевые процессы СПИДа - диссеминированная саркома Капоши (при этом отмечают не только дерматологические признаки, но и поражения внутренних органов) и первичные неходжкинские лимфомы головного мозга (реже - другой локализации).
Этиологию вторичных заболеваний, осложняющих 4-ю стадию ВИЧ-инфекции, во многом определяют бытовые, климатические и природные условия проживания больного ВИЧ-инфекцией.
Диагноз стадии 4В может быть поставлен на основании выраженных признаков энцефалопатии или кахексии - результата непосредственного действия вируса на ЦНС и органы пищеварительной системы. К таким признакам относят значительную непроизвольную потерю массы тела (более 10% от первоначальной), наличие хронической диареи и лихорадки (интермиттирующей или постоянной) на протяжении месяца и более, а также хроническую слабость. При этом оппортунистические инфекции или новообразования нередко отсутствуют.
В этот период развивается тромбоцитопения и глубокая иммуносу-прессия. Количество Т-лимфоцитов составляет <700-800 мкл-1, CD4+-лимфоцитов - <200 мкл-1, происходит резкое уменьшение числа CD8+-лимфоцитов до 400-500 мкл-1. Отношение количества cD4+/CD8+-лимфоцитов не превышает 0,3. При уменьшении количества CD4+-лимфоцитов до 50 мкл-1 возрастает вероятность летального исхода. Развивается несостоятельность системы гуморального иммунитета. Болезнь прогрессирует, наступает терминальная, 5-я стадия, заканчивающаяся фатально.
Осложнения
Осложнениями ВИЧ-инфекции считают вторичные заболевания, развивающиеся на фоне иммунодефицита. Механизм их возникновения связан либо с угнетением клеточного и гуморального иммунитета (инфекционные болезни и опухоли), либо с прямым воздействием ВИЧ (например, поражения ЦНС).
Микобактериозы
Примерно у 65% больных ВИЧ-инфекцией диагностируют туберкулез как впервые возникшее заболевание, у остальных пациентов обнаруживают реактивацию процесса. ВИЧ существенно влияет на состояние иммунной системы (и на иммунореактивность) при туберкулезе, нарушает дифференцировку макрофагов и препятствует образованию специфических гранулем. В то время как на ранних стадиях ВИЧ-инфекции морфология специфического воспаления существенно не меняется, на стадии СПИДа гранулемы просто не формируются. Особенность туберкулеза легких у больных ВИЧ-инфекцией - тяжелое течение заболевания с поражением бронхов и образованием свищей плевры, перикарда и ЛУ. Как правило, в 75-100% случаев у больных ВИЧ-инфекцией развивается легочная форма туберкулеза, однако по мере нарастания иммунодефицита у 25-70% пациентов отмечают диссеминацию и развитие внелегочных форм заболевания. Туберкулез - одна из основных причин смерти пациентов в России на стадии 4В (СПИД).
Процессы, происходящие в легких больных СПИДом людей, - формирование корневой аденопатии и милиарных высыпаний; возникновение преимущественно интерстициальных изменений и образование плеврального выпота. При этом отмечают снижение количества случаев, сопровождающихся распадом легочной ткани, а следовательно, и числа больных, в мокроте которых при микроскопии и посеве обнаруживают микобактерии туберкулеза. Весьма характерным считают частое развитие туберкулезной микобактериемии у больных СПИДом, как правило, осложненной септическим шоком и нарушением функций различных органов. Нередко наблюдают поражение ЛУ (особенно шейных), костей, ЦНС, мозговых оболочек и органов пищеварительной системы; описаны абсцессы простаты и печени. Примерно у 60-80% ВИЧ-инфицированных пациентов туберкулез протекает только с поражением легких, у 30-40% выявляют изменения других органов.
Группу возбудителей «нетуберкулезных» микобактериозов составляют представители различных видов микобактерий. Заболевания у человека вызывают 18 разновидностей микобактерий, 4 вида микроорганизмов обладают сравнительно высокой патогенностью для людей, а 14 видов относят к условно-патогенным. Атипичный микобактериоз, вызванный M. avium (входят в состав комплекса M. avium complex - МАС), - суперинфекция, составляющая группу СПИД-ассоциированных оппортунистических инфекций. До пандемии ВИЧ-инфекции атипичный микобактериоз диагностировали крайне редко, как правило, у лиц с выраженной иммуносупрессией (например, при трансплантации органов и тканей, после длительной кортикостероидной терапии, у онкологических больных). У пациентов, страдающих ВИЧ-инфекцией, иногда развивается диссеминированная форма МАС- инфекции. В терминальной стадии регистрируют локализованную или генерализованную формы заболевания. При локализованной МАС-инфекции обнаруживают абсцессы кожи и поражения ЛУ, а при генерализованной - общеинтоксикационный и желудочно-кишечный синдромы, а также синдром экстрабилиарной обструкции. Признаки общеинтоксикационного синдрома - лихорадка, астенизация, снижение массы тела, тяжелая анемия, лейкопения, повышение активности аланиновой трансаминазы в сыворотке крови. При желудочнокишечном синдроме возникает хроническая диарея, боли в животе; отмечают гепатоспленомегалию, мезаденит и синдром мальабсорбции. Экстрабилиарная обструкция обусловлена перипортальным и перипанкреатическим лимфаденитом, приводящим к билиарному блоку и токсическому гепатиту. Основой диагностики атипичных микобактериозов считают выделение гемокультуры микобактерий. Пневмоцистная пневмония
Возбудитель - P. jirovecii. Инфицирование происходит воздушно-капельным, аэрогенным, ингаляционным и трансплацентарным путем (редко). Пневмоцисты обладают высокой тропностью к легочной ткани, поэтому даже в фатальных случаях патологический процесс редко выходит за пределы легких (это связывают с крайне низкой вирулентностью возбудителя). Клинические формы пневмоцистоза - интерстициальная пневмония и реактивный альвеолит. Симптомы неспецифичны. Продолжительность инкубационного периода пневмоцистной пневмонии от 8-10 дней до 5 нед. Начало заболевания трудно отличить от других инфекций респираторного тракта. Характерно раннее появление одышки (частота дыхательных движений до 3050 в минуту), которая сопровождается сухим или влажным кашлем со скудной, вязкой (иногда пенистой) мокротой, цианозом, повышением температуры тела. Плевральные боли и кровохарканье возникают редко. При аускультации выслушивают жесткое или ослабленное дыхание (локально или над всей поверхностью легких), сухие хрипы. По мере прогрессирования пневмонии могут нарастать симптомы дыхательной и сердечно-сосудистой недостаточности. Рентгенологическая картина вначале неспецифическая, затем обнаруживают прикорневое снижение пневматизации легочной ткани и усиление интерстициального рисунка. Более чем в половине случаев визуализируют билатеральные облаковидные инфильтраты (симптом «бабочки»), а в разгаре заболевания - обильные очаговые тени («ватное» легкое). В дальнейшем на рентгенограммах определяют преимущественно паренхиматозную пневмонию. В 10-30% случаев отмечают асимметричные, как правило, верхнедолевые инфильтраты. При проведении КТ обнаруживают периферические инфильтраты (иногда с очагами распада), снижение прозрачности («матовое стекло») и эмфизематозные участки. Пневмоторакс - наиболее часто возникающее осложнение.
При исследовании крови определяют гипохромную анемию, лейкоцитоз (до 50х109/л) и эозинофилию. При проведении биохимического анализа крови обнаруживают повышение активности ЛДГ до 700-800 МЕ/л. Определение РаО2 позволяет выявить артериальную гипоксемию. Диагноз подтверждают обнаружением пневмоцист в мокроте, лаваже бронхов с помощью различных методов (иммунофлюоресценция, окрашивание образцов по Романовскому-Гимзе и Граму), а также проводят ПЦР- диагностику.
Открытую биопсию легкого выполняют при прогрессирующем течении заболевания. Макроскопически во время операции легкое больного выглядит увеличенным, уплотненным, консистенция его напоминает резину; отмечают буллезные и эмфизематозные изменения, обнаруживают полости распада. Интраальвеолярный пенистый экссудат, диффузные альвеолярные повреждения, эпителиоидные гранулемы, десквамативный интерстициальный пневмонит, интерстициальные лимфоидные инфильтраты - гистологические изменения в ткани легкого при пневмоцистной пневмонии. Выживаемость больных СПИДом при развитии пневмоцистной пневмонии не превышает 55%. Прогноз значительно ухудшается, если лечение начинают на фоне ОДН, тяжелой гипоксии или при лейкопении. Летальность у больных СПИДом составляет от 52,5 до 100%, а при осуществлении ИВЛ - 58-100%.
Цитомегаловирусная инфекция
ЦМВИ, как правило, протекает латентно. Однако иногда диагностируют клинически выраженные формы заболевания, обусловленные первичным инфицированием ЦМВ, а также реинфекцией или реактивацией вируса в зараженном организме. Генерализованная ЦМВИ, сопровождающаяся появлением клинических симптомов, занимает важное место в структуре оппортунистических заболеваний ВИЧ- инфицированных. Ее регистрируют у 20-40% больных СПИДом, не принимающих антиретровирусные препараты. ЦМВИ - непосредственная причина смерти 10-20% ВИЧ-инфицированных. Вероятность возникновения и тяжесть течения ЦМВИ связывают со степенью иммуносупрессии. Если количество CD4+-лимфоцитов в крови составляет 100-200 мкл-1, то манифестную ЦМВИ диагностируют у 1,5% ВИЧ- инфицированных. При уменьшении числа CD4+-лимфоцитов до 50-100 мкл-1 вероятность развития ЦМВИ увеличивается почти в 4 раза. При тотальном снижении СD4+-лимфоцитов (<50 мкл-1) заболевание регистрируют практически у половины инфицированных пациентов. Если содержание CD4+-лимфоцитов в крови достаточно велико (>200 мкл-1), то манифестацию ЦМВИ отмечают редко. ЦМВИ, как правило, развивается постепенно, при этом обнаруживают симптомы-предвестники, предшествующие формированию выраженных органных нарушений. У взрослых отмечают длительную волнообразную лихорадку неправильного типа с подъемами температуры тела выше 38,5 °С, слабость, быструю утомляемость, потерю аппетита, существенное снижение веса; реже - потливость (преимущественно по ночам), артралгии или миалгии. При поражении легких появляется постепенно усиливающийся сухой или со скудной мокротой кашель. На аутопсии обнаруживают фиброателектаз легких с кистами и инкапсулированными абсцессами. Наиболее тяжелый признак ЦМВИ - ретинит (диагностируют у 25-30% пациентов). Больные жалуются на плавающие пятна перед глазами, затем происходит снижение остроты зрения. Потеря зрения необратима в результате воспаления и некроза сетчатки. При ЦМВ-эзофагите у больного при глотании возникает боль за грудиной. При эндоскопии в типичном случае визуализируют обширную поверхностную язву слизистой оболочки пищевода или желудка. Гистологические методы позволяют обнаружить клетки цитомегалии (гигантские многоядерные клетки с внутриядерными включениями) в биоптате; с помощью метода ПЦР можно определить ДНК вируса. ЦМВ может поражать различные органы пищеварительной системы, но чаще развивается колит. Пациента беспокоят боли в животе, жидкий стул, похудание и потеря аппетита. Перфорация кишки - наиболее грозное осложнение. Как возможные клинические симптомы ЦМВИ диагностируют также восходящий миелит и полиневропатию (подострого течения); энцефалит, характеризующийся деменцией; ЦМВ-гепатит с одновременным поражением желчных путей и развитием склерозирующего холангита; адреналит, проявляющийся резкой слабостью и снижением АД. Иногда возникает эпидидимит, цервицит, панкреатит.
Специфическое поражение сосудов преимущественно микроциркуляторного русла и сосудов мелкого калибра - морфологическая особенность патологического процесса при ЦМВИ. Для постановки клинического диагноза «ЦМВИ» необходимо проводить лабораторные исследования. Наличие в крови больного антител класса IgM (или высоких титров антител класса IgG), а также присутствие ДНК вируса в слюне, моче, сперме и вагинальном секрете недостаточно для подтверждения диагноза манифестной ЦМВИ. Обнаружение вируса (его антигенов или ДНК) в крови имеет диагностическое значение. Достоверным критерием высокой активности ЦМВ, доказывающим его этиологическую роль в развитии тех или иных клинических симптомов, служит вирусная нагрузка ЦМВ. При повышении вирусной нагрузки в плазме в 10 раз вероятность развития ЦМВИ возрастает в 3 раза. Определение высокой концентрации ДНК вируса в лейкоцитах крови и плазме требует безотлагательного начала этиотропной терапии.
Токсоплазмоз
Токсоплазмоз - заболевание, вызываемое T. gondii, чаще всего возникающее при уровне CD4+-лимфоцитов <100 мкл 1. Попадание токсоплазм в организм человека приводит к формированию объемных образований в ЦНС (в 50-60% случаев) и появлению первичных эпилептических припадков (в 28% случаев). Токсоплазма - внутриклеточный паразит; заражение человека происходит при употреблении в пищу продуктов (мясо и овощи), содержащих ооцисты или тканевые цисты. Полагают, что развитие токсоплазмоза - реактивация латентной инфекции, поскольку при наличии в сыворотке крови антител к токсоплазме вероятность возникновения токсоплазмоза увеличивается в 10 раз. Однако примерно у 5% ВИЧ-инфицированных на момент постановки диагноза токсоплазмоза антитела к T. gondii отсутствуют. Заражение обычно происходит в детском возрасте. Цисты токсоплазм сохраняются до 10-15 лет, преимущественно в тканях головного мозга и органа зрения, а также во внутренних органах. Патоморфологические изменения при токсоплазмозе имеют фазовый характер. В паразитемической фазе токсоплазмы поступают в регионарные ЛУ, затем проникают в кровеносное русло и распространяются по органам и тканям. Во 2-й фазе происходит фиксация токсоплазм в висцеральных органах, приводящая к развитию некротических и воспалительных изменений и образованию мелких гранулем. В течение третьей (заключительной) стадии токсоплазмы в тканях формируют истинные цисты; воспалительная реакция исчезает, очаги некроза подвергаются обызвествлению. Хотя токсоплазмы могут поражать все органы и ткани, как правило, у ВИЧ-инфицированных регистрируют церебральную форму заболевания. Отмечают лихорадку, головные боли, в 90% случаев разнообразную очаговую неврологическую симптоматику (гемипарез, афазия, психические и некоторые другие нарушения). При отсутствии адекватного лечения развиваются спутанность сознания, оглушенность, сопор и кома в результате отека головного мозга. При выполнении МРТ или КТ с контрастированием обнаруживают множественные очаги с кольцевидным усилением и перифокальным отеком, реже - единичный очаг. Дифференциальную диагностику проводят с лимфо-мой головного мозга, опухолями другой этиологии, СПИД-дементным синдромом, мультифокальной лейкоэнцефалопатией и туберкулемами. Почти в каждом случае диагностируют преимущественное поражение определенных органов и систем. Иногда токсоплазмоз протекает без формирования объемных образований в головном мозге (по типу герпетического энцефалита или менингоэнцефа-лита). Внемозговые локализации токсоплазмоза (например, интерстициальная пневмония, миокардит, хориоретинит и поражение органов пищеварительной системы) у ВИЧ-инфицированных с выраженным иммунодефицитом регистрируют в 1,5-2% случаев. Максимальное количество очагов внемозговой локализации обнаруживают при исследовании зрительного аппарата глаза (примерно в 50% случаев). Диссеминация (по меньшей мере две локализации) происходит в 11,5% случаев. Диагностировать токсоплазмоз крайне сложно. Ликвор при спинномозговой пункции может быть интактным. Диагноз токсоплазмоза устанавливают на основании клинической картины, данных МРТ или КТ, а также при наличии антител к токсоплазме в сыворотке крови и ДНК токсоплазмы в биоматериале.
Саркома Капоши
Саркома Капоши - многоочаговая сосудистая опухоль, поражающая кожу, слизистые оболочки и внутренние органы. Развитие саркомы Капоши связывают с HHV-8, который впервые обнаружили в коже больного с этой опухолью. В отличие от эндемического и классического вариантов заболевания, эпидемическую форму саркомы регистрируют только у ВИЧ-инфицированных (преимущественно у гомосексуалов).
В патогенезе саркомы Капоши ведущую роль отводят не злокачественному перерождению клеток, а нарушению продукции цитокинов, контролирующих клеточную пролиферацию. Инвазивный рост для данной опухоли нехарактерен. При гистологическом исследовании саркомы Капоши обнаруживают усиленную пролиферацию веретенообразных клеток, сходных с эндотелиальными и гладкомышечными клетками сосудов. Саркома у ВИЧ-инфицированных протекает неодинаково. У одних больных диагностируют легкую форму заболевания, у других - более тяжелую. Клинические признаки саркомы Капоши разнообразны. Чаще всего развиваются поражения кожи, ЛУ, органов пищеварительной системы и легких. Разрастание опухоли может приводить к лимфатическому отеку окружающих тканей. В 80% случаев поражение внутренних органов сочетается с вовлечением в патологический процесс кожи. На начальных стадиях заболевания на коже или слизистой оболочке формируются небольшие возвышающиеся красно-лиловые узлы, нередко возникающие на месте травмы. Вокруг узловых элементов иногда обнаруживают мелкие темные пятна или желтоватый ободок (напоминают синяки). Диагноз саркомы Капоши ставят с учетом гистологических данных. При биопсии пораженных участков отмечают пролиферацию веретенообразных клеток, диапедез эритроцитов; обнаруживают содержащие гемосидерин макрофаги, а также воспалительные инфильтраты. Одышка - первый признак поражения легких при саркоме Капоши, иногда наблюдают кровохарканье. На рентгенограммах грудной клетки определяют двусторонние затемнения в нижних долях легких, сливающиеся с границами средостения и контуром диафрагмы; нередко обнаруживают увеличение прикорневых ЛУ. Саркому Капоши следует дифференцировать с лимфомами и микобактериальной инфекцией, протекающей с поражением кожи. У 50% больных диагностируют поражение органов пищеварительной системы, а в тяжелых случаях возникает кишечная непроходимость или кровотечение. Вовлечение в патологический процесс желчных путей приводит к развитию подпеченочной желтухи.
Летальность и причины смерти
Смерть больных ВИЧ-инфекцией наступает либо от прогрессирования вторичных заболеваний, либо от любых других сопутствующих заболеваний, не связанных с ВИЧ. Генерализованный туберкулез - основная причина гибели больных СПИДом. Кроме ТОГО, причиной смерти считают легочную патологию (с последующим развитием ДН) и манифестную ЦМВИ. В последнее время регистрируют увеличение летальности вследствие цирроза печени, обусловленного наличием ХГС на фоне хронической алкогольной интоксикации. Прогрессирование хронического гепатита в цирроз у таких пациентов происходит в течение 2-3 лет.
ДИАГНОСТИКА
Клиническая диагностика
Для диагностики ВИЧ-инфекции необходимо лабораторное подтверждение. Проводят клиническую диагностику вторичных или сопутствующих заболеваний на фоне ВИЧ- инфекции; это позволяет определить тяжесть состояния больного, показания к госпитализации и тактику лечения.
Специфическая и неспецифическая лабораторная диагностика
Для подтверждения диагноза ВИЧ-инфекции используют вирусологический, молекулярно-генетический (ПЦР) и серологические методы (ИФА) и ИБ.
Антитела к ВИЧ определяют через 2 нед с момента заражения. При регистрации первого положительного результата ИФА повторяют. После получения второго положительного ответа данную сыворотку крови направляют на исследование в территориальный центр профилактики и борьбы со СПИДом, где проводят ИБ, результаты которого оценивают как положительные, сомнительные или отрицательные.
При обнаружении в сыворотке крови пациента антител к любым двум или трем гликопротеинам оболочки ВИЧ (gp41, gp120 и gp160) одновременно пробы считают положительными. При отсутствии в сыворотке крови антител ко всем антигенам пробы оценивают как отрицательные. Если в крови обнаруживают антитела к одному гликопротеину ВИЧ или каким-либо другим его протеинам, пробы считают сомнительными, требующими проведения повторного исследования.
Выделение и идентификация культуры ВИЧ (вирусологический метод) - достоверный критерий оценки инфицирования. В силу сложности проведения данное исследование используют в научных целях в исключительно трудных для диагностики случаях.
Количественный анализ в ПЦР позволяет оценить репликативную активность вируса; определить «вирусную нагрузку». В стадии первичных проявлений «вирусная нагрузка» составляет обычно несколько тысяч копий в 1 мл крови. В стадии вторичных заболеваний концентрация ВИЧ достигает сотен тысяч копий в 1 мл сыворотки крови и миллиона копий вируса в стадии 4В.
Стойкая высокая концентрация ВИЧ на ранней стадии болезни - неблагоприятный прогностический признак, свидетельствующий о высокой вирулентности штамма.
Первичная диагностика ВИЧ-инфекции - ответственная процедура, требующая тщательного анализа данных, ибо постановка неправильного диагноза может иметь тяжелые последствия для больного (депрессивная реакция, суицидальная попытка, СПИДофобия).
Стандарт диагностики
Обнаружение в ИФА антител к ВИЧ с последующим подтверждением их специфичности ИБ - стандартная процедура.
Показания к консультациям других специалистов
Перед началом АРТ всех пациентов с ВИЧ-инфекцией осматривает терапевт, невролог, оториноларинголог и офтальмолог для определения противопоказаний к назначению тех или иных препаратов. Кроме того, больных, употреблявших ранее или применяющих постоянно психоактивные вещества, направляют на консультацию к наркологу. Всех пациентов с легочной патологией, особенно при неэффективности антибактериальной терапии, осматривает фтизиатр. Консультации других специалистов осуществляют по показаниям, в зависимости от выявленной патологии (вторичных или сопутствующих заболеваний), для определения объема дополнительных обследований или решения вопроса о переводе больного в узкоспециализированное отделение или стационар.
Пример формулировки диагноза
При постановке диагноза указывают нозологическую единицу заболевания - ВИЧ- инфекция по МКБ-10, затем - стадию ВИЧ-инфекции, вторичные заболевания и фазу. Если на фоне ВИЧ-инфекции хотя бы одно из вторичных заболеваний имеет степень проявления, соответствующую критериям СПИДа, то после стадии заболевания указывают «(СПИД)».
Например
Z21 Бессимптомный инфекционный статус, вызванный вирусом иммунодефицита человека (ВИЧ).
ВИЧ-инфекция, стадия 3 (субклиническая).
B20.4 Болезнь, вызванная ВИЧ, с проявлениями кандидоза.
ВИЧ-инфекция, стадия вторичных заболеваний 4А, фаза спонтанной ремиссии: орофарингеальный кандидоз в анамнезе.
B20.6 Болезнь, вызванная ВИЧ, с проявлениями пневмонии, вызванной P. jirovecii.
ВИЧ-инфекция, стадия вторичных заболеваний 4В (СПИД), фаза прогрессирования при отсутствии АРТ: пневмоцистная пневмония, кандидоз полости рта и пищевода.
B20.2 Болезнь, вызванная ВИЧ, с проявлениями цитомегаловирусного заболевания.
ВИЧ-инфекция, стадия вторичных заболеваний 4В (СПИД), фаза ремиссии на фоне АРТ: манифестная ЦМВИ с поражением сетчатки в анамнезе.
Показания к госпитализации
Госпитализацию больных ВИЧ-инфекцией осуществляют с учетом тяжести состояния и клинических данных, в зависимости от наличия вторичных или сопутствующих заболеваний.
ЛЕЧЕНИЕ
Режим и диета
Режим и диету больным назначают соответственно установленным нозологическим формам.
Медикаментозная терапия
Этиотропная терапия
Современный арсенал лекарственных препаратов позволяет подавить репликацию ВИЧ у большей части больных, как правило, на довольно длительный срок и замедлить прогрессирование заболевания в стадию СПИД.
Антиретровирусные препараты, разрешенные к применению в Российской Федерации.
• НИОТ: абакавир, абакавир + ламивудин, диданозин, зидовудин, зидовудин + абакавир + ламивудин, зидовудин + ламивудин, ламивудин, ставудин, тенофо-вир, тенофовир + эмтрицитабин, фосфазид.
• ННИОТ: эфавиренз, невирапин, этравирин, рилпивирин.
• ИП: атазанавир, дарунавир, индинавир, лопинавир + ритонавир, нелфинавир (не используется), ритонавир (практически не используется как ИП, применяют в качестве бустера), саквинавир, типранавир, фосампренавир.
• Ингибиторы фузии (слияния): энфувиртид.
• ИИ: ралтегравир, долутегравир.
• Антагонисты CCR5-рецепторов (АР): маравирок.
• Фиксированная комбинация ННИОТ + НИОТ: рилпивирин + тенофовир + эмтрицитабин (табл. 21.10).
Таблица 21.10. Антиретровирусные препараты, дозы и схемы их применения
|
Препарат |
Дозы и схема применения |
|
Абакавир |
300 мг 2 р/сут или 600 мг 1 р/сут. Перед назначением выполнить HLA-B*5701 скрининг |
|
Абакавир/ламивудин |
600 мг/300 мг 1 р/сут. Перед назначением выполнить HLA-B*5701 скрининг |
|
Атазанавир |
400 мг 1 р/сут |
|
300 мгатаназавираи 100 мгритонавира 1 р/сут |
|
|
Дарунавир |
600 мгдарунавира и 100 мг ритонавира 2 р/сут |
|
800 мгдарунавира и 100 мг ритонавира 1 р/сут |
|
|
Диданозин |
250 или 400 мг 1 р/сут в зависимости от массы тела |
|
Долутегравир |
50 мг 1 р/сут |
|
Зидовудин |
300 мг 2 р/сут |
|
Зидовудин/ламивудин |
300 мг /150 мг 2 р/сут |
|
Зидовудин/абакавир/ламивудин |
300 мг /300 мг /150 мг 2 р/сут. Перед назначением выполнить HLA-B*5701 скрининг |
|
Индинавир |
800 мг индинавира и 100 мг ритонавира 2 р/сут |
|
400 мг индинавира и 200 мг ритонавира 2 р/сут |
|
|
800 мг 3 р/сут |
|
|
Ламивудин |
150 мг 2 р/сут |
|
300 мг 1 р/сут |
|
|
Лопинавир/ритонавир |
400/100 мг2 р/сут |
|
800/200 мг 1 р/сут |
|
|
Маравирок |
300 мг 2 р/сут |
|
150 мг 2 р/сут. В комбинациях с рядом ННИОТ и ИП необходима коррекция доз. Выполнение анализа на тропизм вируса перед началом терапии |
|
|
Невирапин |
200 мг 1 р/сут в течение 14 дней, затем 2 р/сут |
|
Нелфинавир |
750 мг 3 р/сут |
|
1250 мг 2 р/сут |
|
|
Ралтегравир |
400 мг 2 р/сут |
|
Рилпивирин |
25 мг 1 р/сут |
|
Ритонавир |
100 мг или 200 мг 2 р/сут (используют для бустирования других ИП) |
|
Саквинавир |
1000 мг саквинавира и 100 мг ритонавира 2 р/сут |
|
Ставудин |
30 мг 2 р/сут |
|
Тенофовир |
300 мг 1 р/сут |
|
Тенофовир/эмтрицитабин |
300/200 мг 1 р/сут |
|
Тенофовир/эмтрицитабин/рилпивирин |
300/200/25 мг 1 р/сут |
|
Типранавир |
500 мг типранавира и 200 мг ритонавира 2 р/сут |
|
Фосампренавир |
1400 мг 2 р/сут |
|
700 мг фосампренавира и 100 мг ритонавира 2 р/сут |
|
|
1400 мг фосампренавира и 100 мг ритонавира 1 р/сут |
|
|
Энфувиртид |
90 мг 2 р/сут (п/к) |
|
Этравирин |
200 мг 2 р/сут |
|
Эфавиренз |
600 мг 1 р/сут |
Факторы, учитываемые при решении вопроса о назначении антиретровирусных препаратов.
• Степень иммунодефицита (оценивают на основании количества СЮ4+-лимфоцитов).
• Риск прогрессирования болезни (определяют по уровню РНК ВИЧ в крови).
• Готовность и желание пациента начать лечение.
• Возраст пациента.
• Наличие ко-инфекции ВИЧ/ХГВ и/или ВИЧ/ХГС.
• Наличие вторичных и сопутствующих заболеваний, нефропатии.
• Эпидемиологические особенности (дискордантная пара, подготовка пациента к применению вспомогательных репродуктивных технологий).
• Осведомленность пациента о возможных побочных эффектах препаратов и об изменении качества жизни.
• Выбор стартовой терапии для достижения стойкого вирусологического ответа и сохранение максимального выбора комбинаций препаратов для последующего использования.
• Фармакоэкономическая целесообразность выбора различных схем антивирусной терапии (АРВТ).
Для начала АРВТ существуют определенные показания. Разработаны различные схемы применения препаратов (схемы 1-го, 2-го и 3-го ряда), составленные с учетом проведенных клинических исследований эффективности антиретровирусных препаратов (АРВП) (табл. 21.11, 21.12).
Таблица 21.11. Показания к проведению АРВТ (при уровне доказательной базы менее AI решение о необходимости назначения АРВт принимают коллегиально)
|
Клиническая картина |
Количество CD4+- лимфоцитов (мкл-1) |
Концентрация РНК ВИЧ в сыворотке (копий/мл) |
Рекомендации |
|
Наличие вторичных и, особенно, СПИД- индикаторных заболеваний |
Любое значение |
Любое значение |
Начинают или продолжают лечение (AI) |
|
Активная форма туберкулеза |
Любое значение |
Любое значение |
Начинают или продолжают лечение (AIII) |
|
ХГВ, если показано лечение |
Любое значение |
Любое значение |
Начать лечение (AII) |
|
ХГС |
<500 |
Любое значение |
Начать АРТ (CIII), после повышения иммунного статуса присоединяют терапию ХГС |
|
»500 |
Любое значение |
АРТ может быть отложена до завершения курса лечения ХГС |
|
|
Острая ВИЧ-инфекция |
Любое значение |
Любое значение |
Начать лечение (BIII), пожизненно |
|
ВИЧ-ассоциированная нефропатия |
Любое значение |
Любое значение |
Начать лечение (AII) |
|
Заболевания, требующие длительного приема терапии, угнетающей иммунитет |
Любое значение |
Любое значение |
Начать лечение (AIII) |
|
Беременность |
Любое значение |
Любое значение |
Начать (AII) или продолжить лечение |
|
Пациенты старше 60 лет с ВИЧ- ассоциированными нейрокогнитивными расстройствами |
Любое значение |
Любое значение |
Начать лечение (BII) |
|
ВИЧ-инфицированному партнеру в дискордантной паре |
Любое значение |
Любое значение |
Начать лечение (AI) |
Окончание табл. 21.11
|
Клиническая картина |
Количество CD4+- лимфоцитов (мкл-1) |
Концентрация РНК ВИЧ в сыворотке (копий/мл) |
Рекомендации |
|
Подготовка ВИЧ-инфицированного пациента к применению вспомогательных репродуктивных технологий |
Любое значение |
Любое значение |
Начать лечение (AIII) |
|
Бессимптомное течение |
>500 мкл-1 |
<100 000 |
Необходимость назначения АРТ обсуждают коллегиально. Можно начать АРТ при готовности пациента принимать терапию пожизненно. Назначают АРТ при быстром снижении СD4+-лимфоцитов (>100 мкл-1/год) (Аш) |
|
>100 000 |
Начать АРТ (BII). Назначают АРТ при быстром снижении СD4+-лимфоцитов (>100 мкл-1/год) (АШ). |
||
|
Необходимость назначения АРТ обсуждают коллегиально |
|||
|
350-500 |
<100 000 |
Начать лечение (AII) |
|
|
>100 000 |
Начать лечение (BII) |
||
|
<350 |
Любое значение |
Начать лечение (AI) |
Таблица 21.12. Схемы АРТ с использованием препаратов первого ряда
По одному препарату или комбинации из граф А и В (применяют предпочтительную категорию)
|
Схемы выбора |
Графа А |
Графа В |
|
ННИОТ: эфавиренз, рилпивирин |
тенофовир и ламивудин, тенофовир и эмтрицитабин, абакавир и ламивудин (перед началом лечения необходимо провести скрининг HLA-B*5701) |
|
|
ИП: атазанавир/ритонавир, дарунавир/ ритонавир, фосампренавир/ритонавир, лопинавир/ритонавир |
||
|
ИИ: ралтегравир |
||
|
Альтернативные схемы |
ННИОТ: невирапин |
зидовудин и ламивудин |
|
Другие препараты, используемые иногда в терапии 1-го ряда в качестве альтернативной схемы |
зидовудин/ламивудин/абакавир (перед началом лечения необходимо провести скрининг HLA- B*5701) |
|
Возникновение мутантных штаммов вируса - одна из основных причин вирусологической неудачи АРВТ.
Принципы изменения режима АРВТ при неэффективности схемы первого ряда
Наиболее важными принципами выбора препаратов для новой схемы АРВТ при вирусологической неэффективности текущей схемы АРВТ являются следующие: проводить смену АРВТ по результатам теста на резистентность (AII); при наличии возможностей осуществлять замену препаратов внутри фармакологических групп (А11);
включать в схему по крайней мере 2, а лучше 3 АРВП (принадлежащих к >2 фармакологическим группам), которые обладают активностью против данной популяции вируса по результатам проведенных тестов на резистентность;
Л при оценке резистентных свойств вируса следует учитывать результаты всех тестов на резистентность и сведения обо всех принимавшихся ранее АРВП; устранить факторы, препятствовавшие адекватному ответу на прежнюю или текущую схему терапии;
менять схему терапии по причине вирусологической неэффективности следует как можно быстрее во избежание накопления дополнительных мутаций резистентности, сужающих спектр активных АРВП для применения в будущем. Исключения составляют ламивудин и эмтрицитабин; не прерывать АРВТ за исключением случаев тяжелых побочных эффектов; если АРВТ прервана, тест на резистентность назначается не позднее 2 нед перерыва;
не ограничиваться добавлением еще одного АРВП к неэффективной схеме АРВТ.
Схемы лечения пациентов с множественной резистентностью к АРВП
Множественная резистентность к АРВП - это наличие резистентности к препаратам различных фармакологических групп. Лечение пациентов с таким видом резистентности представляет наиболее сложную задачу, требует повышенного внимания врача. Даже при правильно интерпретированных результатах исследования резистентности вируса только опытный специалист по лечению ВИЧ- инфекции должен начинать, прекращать или менять АРВТ.
Рекомендуется следующее.
• Индивидуальный режим наблюдения, более частый клинический и лабораторный мониторинг (BIII).
• Назначение препаратов в соответствии с исследованием профиля резистентности вируса методом секвенирования генома.
• Для лечения больных с множественной резистентностью к АРВП возможно назначение в одной схеме ИП и ННИОТ; ИП, ННИОТ и ИИ; двух ИП с соответствующей коррекцией доз.
• С учетом наименьшего риска мутаций в схемах лечения таких больных - дарунавир/ритонавир в дозировке 600/100 мг 2 р/сут (BII).
• В схемах лечения используются ингибиторы интегразы, ингибиторы слияния, АР.
• В целях быстрого подавления вирусной нагрузки рекомендуется введение в схему энфувиртида в качестве 3-го или 4-го компонента. По достижении вирусологической и иммунологической эффективности проводится переключение с энфувиртидана ралтегравир.
• Симплификация схем лечения больным, у которых была за фиксирована резистентность к антивирусным препаратам, не допускается.
Принцип подхода к лечению пациентов с ВИЧ-инфекцией - пожизненное применение антиретровирусных препаратов.
Патогенетическая терапия и схемы лечения вторичных заболеваний, наиболее часто регистрируемых у ВИЧ-инфицированных пациентов
При лечении больных ВИЧ-инфекцией немаловажную роль играет терапия вторичных и сопутствующих заболеваний. В большинстве случаев лечение таких болезней имеет приоритет перед началом АРВТ, поскольку тяжесть состояния пациента определяет наличие той или иной нозологии.
Цитомегаловирусная инфекция
Лечение манифестной ЦМВИ.
• Проводят 3-недельную терапию ганцикловиром в дозе 5 мг/кг 2 р/сут в/в медленно в течение часа.
• Назначают валганцикловир в дозе 900 мг 2 р/сут внутрь в течение 3 нед (менее предпочтительно).
Лечение и вторичная профилактика активной ЦМВИ.
• Применяют валганцикловир внутрь по 900 мг 1 р/сут в течение 30 дней.
• Проводят 4-недельную терапию ганцикловиром по 5 мг/кг 1 р/сут в/в капельно в течение часа (менее предпочтительно).
ГИ, вызванная ВПГ 3-го типа (Varicella-Zoster), лечение проводят не менее 10 дней.
• Назначают ацикловир по 800 мг 5 р/сут (внутрь) или по 750-1000 мг 3 р/сут (в/в).
• Применяют валацикловир по 1 г 3 р/сут (внутрь).
• Используют фамцикловир по 500 мг 3 р/сут в течение 7-10 дней (внутрь). Пневмоцистная пневмония
Схема выбора.
• Триметоприм/сульфаметоксазол, 5/25 мг/кг внутрь или в/в капельно каждые 6 ч в течение 28 сут.
Альтернативные схемы.
• Клиндамицин в дозе 600-900 мг в/в каждые 6-8 ч.
Первичная и вторичная профилактика пневмоцистной пневмонии (при уровне CD4+- лимфоцитов <200 мкл-1): триметоприм/сульфаметоксазол, 80/400 мг 2 р/сут через день до повышения количества CD4+-лимфоцитов >200 мкл-1. При непереносимости триметоприма/сульфаметоксазола используют дапсон, 100 мг внутрь 1 р/сут. При рО2 <70 мм рт.ст. или альвеолярно-артериолярном градиенте по кислороду >35 мм рт.ст. назначается преднизолон 1 мг/кг с последующим уменьшением дозы, а также оксигенотерапия до повышения количества CD4+-лимфоцитов >200 мкл-1.
Токсоплазмоз (чаще диагностируют церебральную форму)
Лечение токсоплазмоза начинают при малейшем подозрении на данное заболевание, не дожидаясь результатов обследования.
Схема выбора.
• Пириметамин/сульфадоксин (25/500 мг), 200 мг (8 таблеток) из расчета по пириметамину в 1-й день, далее 50 мг (при массе тела <60 кг) или 75 мг (при массе тела >60 кг) в сутки в сочетании с фолинатом кальция (по 25 мг) в/м не менее 6 нед (до элиминации не менее 75% очагов на МРТ головного мозга).
Альтернативные схемы.
Триметоприм/сульфаметоксазол, 5/25 мг/кг внутрь или в/в капельно 2 р/сут не менее 6 нед (до элиминации не менее 75% очагов на МРТ головного мозга). Вторичная профилактика токсоплазмоза - половинные дозы лечебного курса в течение 6 мес после достижения уровня CD4+-лимфоцитов >200 мкл-1.
Саркома Капоши
АРТ - основной метод, позволяющий предотвратить прогрессирование заболевания и добиться клинического улучшения. При тяжелой форме саркомы Капоши, протекающей с вовлечением в патологический процесс внутренних органов, назначают проспидия хлорид в дозе 100 мг в/м в течение 30 сут; или доксоруби-цин липосомальный в дозе 20 мг/м2, повторяют через 2-3 нед; или даунорубицин липосомальный в дозе 40 мг/м2, повторяют через 2-3 нед.
Кандидозный стоматит
Схема выбора.
• Флуконазол 100 мг внутрь 1 р/сут до достижения клинического эффекта. Альтернативные схемы.
• Флуконазол по 100 мг/сут до исчезновения симптомов.
• Нистатин в дозе 500 000 ЕД 5 р/сут.
• Кетоконазол 200 мг внутрь 1 р/сут.
Кандидозный эзофагит
Схема выбора.
• Флуконазол в дозе 400 мг в 1-е сутки, далее 200 мг/сут внутрь в течение 2-3 нед.
Альтернативные схемы.
• Итраконазол 100-200 мг 2 р/сут в течение 2-3 нед.
• Амфотерицин В 0,3-0,7 мг/кг/сут в/в капельно в течение 5-7 сут.
• Вориконазол, с учетом рекомендуемой насыщающей дозы. Криптококковая инфекция с поражением центральной нервной системы
Схема выбора.
• Амфотерицин B [липидный комплекс] (Амфолип*), амфотерицин B [холестерилсульфатный комплекс] (Амфоцил*) 0,7 мг/кг/сут в/в капельно в сочетании с 5- флуцитзином*э внутрь по 100 мг/кг/сут в течение 4-6 нед (индукционная схема). Затем назначают флуконазол в дозе 400 мг/сут в течение 2 мес или до санации ликвора. Заключительный этап - поддерживающая терапия флуконазолом (200 мг/сут) до повышения количества СD4+-лимфоцитов >200 мкл 1.
Альтернативные схемы.
• Амфотерицин В в дозе 0,7-1,0 мг/кг/сут в/в в течение 2 нед в сочетании с флуконазолом внутрь по 400 мг/сут в течение 8-10 нед.
• Итраконазол по 200 мг 2 раза в день в течение до 8 нед.
• Флуконазол внутрь по 400-800 мг/сут в комбинации с 5-флуцитзином*а внутрь по 100 мг/кг/сут в течение 6-10 нед.
• Используют амфотерицин В липосомальный по 4 мг /кг/сут в/в капельно в течение 2 нед. Затем флуконазол по 400 мг/сут в течение 8-10 нед.
• Вориконазол, с учетом рекомендуемой насыщающей дозы. Микобактериальная инфекция
При лечении микобактериозов, обнаруженных у ВИЧ-инфицированных, назначают стандартные препараты и используют обычные схемы дозирования.
Особенности терапии микобактериальной инфекции у ВИЧ-инфицированных пациентов.
• При уменьшении количества CD4+-лимфоцитов (<100 мкл-1) пациентам назначают рифампицин или рифабутин не реже 3 раз в неделю, поскольку более редкий прием препаратов приводит к формированию резистентности возбудителя. Длительность лечения определяют индивидуально.
• При сильном снижении количества CD4+-лимфоцитов (<50 мкл-1) для терапии туберкулеза используют не менее 4 препаратов в течение 2 мес; затем оставляют 2 препарата (их применяют в течение 4,5 мес). Если при анализе мокроты после 2 мес лечения получают положительные результаты, то терапию проводят в течение последующих 7 мес.
• При обнаружении внелегочных форм туберкулеза назначают стандартные схемы лечения туберкулеза легких. Исключение составляют милиарный туберкулез, туберкулез костей и суставов, туберкулезный менингит (лечение проводят в течение 12 мес).
• Нельзя одновременно начинать лечение туберкулеза и ВИЧ-инфекции вследствие наложения побочных эффектов используемых препаратов, неблагоприятных лекарственных взаимодействий, требований к соблюдению режима приема препаратов и вероятности парадоксальных реакций, связанных с восстановлением иммунной системы. АРТ и противотуберкулезное лечение можно начинать одновременно при резком уменьшении CD4+-лимфоцитов до 50 мкл-1 (если пациент хорошо переносит противотуберкулезную терапию).
• Не рекомендуют при проведении противотуберкулезной терапии использовать ИП и ННИОТ, за исключением эфавиренза, ритонавира и комбинации ритонавира и саквинавира.
Гепатит
Принципы лечения ХГС у больных ВИЧ-инфекцией соответствуют таковым у пациентов без ВИЧ-инфекции. ХГС у больных ВИЧ-инфекцией может приводить к увеличению частоты и скорости прогрессии цирроза печени, печеночно-клеточному раку, высокому риску повышения активности аминотрансфераз на фоне АРТ.
Лечение ГС показано всем ВИЧ-инфицированным с ВИЧ/ХГС (при наличии РНК ВГС в крови).
Начальный этап противовирусной терапии ХГС у больных ВИЧ-инфекцией представлен в таблице (табл. 21.13).
Таблица 21.13. Начальные этапы противовирусной терапии хронического вирусного гепатита С у пациентов с ВИЧ-инфекцией
|
Количество CD4+- лимфоцитов (мкл- 1) |
Принципы лечения ХГС и ВИЧ-инфекции |
|
<500 |
АРТ целесообразно провести до начала лечения ХГС, учитывая высокий риск возникновения оппортунистических инфекций, а также возможность снижения числа С04*-лимфоцитов на фоне интерферонотерапии. Только после стабилизации ВИЧ-инфекции (то есть в отсутствие вторичных заболеваний, лечение которых является приоритетным), а также повышения уровня С04*-лимфоцитов >200 мкл-1 и подавления РНК ВИЧ можно начать терапию ХГС |
|
>500 |
Риск прогрессии инфекции невысок, и АРТ можно отсрочить. Наиболее предпочтительно начать лечение ХГС |
В настоящее время появились новые препараты с прямым противовирусным действием в отношении ВГС которые могут применяться без ИФН (± рибавирин) и способны привести к элиминации HCV за 12-24 нед в зависимости от исходного состояния печени. Из всего имеющегося спектра таких препаратов в Российской Федерации в настоящее время зарегистрированы препараты для лечения только при инфекции, вызванной 1-м генотипом ВГС К ним относятся:
1) интерфероновые схемы: симепревир, который используется в сочетании с пэгилированным ИФН-а и рибавирином;
2) безинтерфероновые схемы: омбитасвир + паритапревир + дасабувир + ритонавир, даклатасвир, асунапревир.
Лечение такими препаратами и используемые схемы аналогичны как у больных без ВИЧ-инфекции, так и у ВИЧ-инфицированных. Однако при одновременном лечении ВИЧ-инфекции и ВГС с использованием безинтерфероновых схем следует учитывать межлекарственные взаимодействия.
Назначение иммуноглобулинов больным ВИЧ-инфекцией можно рассматривать как патогенетическую терапию.
Показания к применению иммуноглобулинов.
• Иммунодефицит (с заместительной целью).
• Идиопатические тромбоцитопении с аутоиммунным механизмом развития (по 20 г белка в сутки).
• Тяжелые бактериальные и вирусные вторичные и сопутствующие заболевания.
Дозы препаратов и курс лечения зависят от степени иммунодефицита, тяжести состояния пациента, а также препарата группы иммуноглобулинов.
Медико-социальная экспертиза
При проведении медико-социальной экспертизы ВИЧ-инфицированных учитывают выраженность клинических признаков заболевания (стадию ВИЧ-инфекции). Социальные причины - невозможность дальнейшего выполнения работы (например, хирург, стоматолог, акушер-гинеколог, реаниматолог, медицинский персонал, производящий парентеральные манипуляции, работники станции переливания крови и заводов биомедицинских препаратов, в профессиональную обязанность которых входит приготовление препаратов для парентерального введения) - основание для определения стойкой утраты трудоспособности.
В случае невозможности профессиональной переориентации указанных лиц может быть оформлена III группа инвалидности.
Вопросы временной нетрудоспособности решают строго индивидуально, на основании тяжести и продолжительности различных клинических признаков, руководствуясь «Инструкцией о правилах экспертизы временной нетрудоспособности для застрахованных лиц», с последующими дополнениями и исправлениями.
Для определения степени стойкой утраты трудоспособности больных ВИЧ-инфекцией используют индекс Карновского.
• Если индекс Карновского составляет 100-90%, то активность пациента полностью сохранена.
• Способность пациента к напряженной физической работе ограничена (может выполнять легкую работу) при значении индекса 80-70%.
• Если величина индекса Карновского не превышает 60-30%, то пациент способен передвигаться и ухаживать за собой, но не может работать (лежит или сидит менее 50% периода бодрствования).
• Ограничение способности ухаживать за собой, пациент лежит или сидит более 50% времени бодрствования - значение индекса составляет 40-30%.
• Индекс Карновского не превышает 20-10%; при этом больной полностью обездвижен и не может ухаживать за собой.
В течение стадии первичных клинических проявлений ВИЧ-инфекции (стадии 2 и 3) трудоспособность пациентов полностью сохранена (индекс Карновского - 90-100%).
На стадии вторичных заболеваний (стадия 4А) трудоспособность больных также сохранена полностью (индекс Карновского - 90-100%). Вместе с тем у некоторых пациентов отмечают развитие стойких астенических расстройств и формирование психоорганического синдрома; это приводит к снижению способности к трудовой деятельности в полном объеме (индекс Карновского - 70-80%). В таком случае, учитывая характер профессиональной деятельности, рекомендуют оформить больному III группу инвалидности.
На более поздних стадиях ВИЧ-инфекции (стадия 4Б) отмечают учащение рецидивов вторичных заболеваний и возникает необходимость в госпитализации (неоднократно) большинства больных, что приводит к стойкой утрате трудоспособности (индекс Карновского - 50-80%). В таком случае пациента переводят на II или III группу инвалидности. Исключение составляют стойкие поражения ПНС с выраженными нарушениями двигательных функций (индекс Карновского составляет 10-40%). Пациенту оформляют I группу инвалидности.
На стадии вторичных заболеваний (стадия 4В) у всех больных обнаруживают стойкое нарушение трудоспособности (индекс Карновского - 10-50%). В зависимости от характера и тяжести поражений рекомендуют устанавливать I или II группу инвалидности.
Диспансеризация
В Российской Федерации Федеральным законом от 30 марта 1995 г. № 38-ФЗ «О предупреждении распространения в Российской Федерации заболевания, вызываемого вирусом иммунодефицита человека (ВИЧ-инфекции)» закреплены принципы:
бесплатного лекарственного обеспечения больных ВИЧ-инфекцией в амбулаторных условиях (п. 1 ст. 4 Федерального закона № 38-ФЗ);
˄ запрета дискриминации при оказании медицинской помощи в специализированных и неспециализированных медицинских организациях в равной степени частной и государственной систем здравоохранения (ст. 14 Федерального закона № 38-ФЗ).
С принятием Федерального закона от 21 ноября 2011 г. № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» медицинская помощь и лекарственное обеспечение осуществляются в соответствии с порядками и стандартами оказания медицинской помощи по профилю соответствующего заболевания.
С целью организации медицинской помощи больным ВИЧ-инфекцией и для увеличения продолжительности и улучшения качества их жизни, а также для проведения противоэпидемических мероприятий необходимо обеспечить максимальный охват диспансерным наблюдением ВИЧ-инфицированных пациентов.
Все обследования ВИЧ-инфицированного пациента выполняют только после получения добровольного информированного согласия. Рекомендуют активно приглашать ВИЧ-инфицированных пациентов на периодические обследования, но при этом нельзя нарушать права людей на отказ от обследования и лечения. Пациент также имеет право на выбор медицинского учреждения.
Диспансеризацию ВИЧ-инфицированных пациентов проводят, руководствуясь нормативными документами.
• Порядок оказания медицинской помощи взрослому населению при заболевании, вызываемом вирусом иммунодефицита человека (ВИЧ-инфекции) (утвержден приказом Минздрава России от 8 ноября 2012 г. № 689н).
• Порядок оказания медицинской помощи по профилю «акушерство и гинекология» (за исключением использования вспомогательных репродуктивных технологий) (утвержден приказом Минздрава России от 1 ноября 2012 г. № 572н).
• Стандарт специализированной медицинской помощи при болезни, вызванной вирусом иммунодефицита человека (ВИЧ-инфекции) (утвержден приказом Минздрава России от 9 ноября 2012 г. № 758н).
• Стандарт первичной медико-санитарной помощи при болезни, вызванной вирусом иммунодефицита человека (ВИЧ-инфекции) (утвержден приказом Минздрава России от 24 декабря 2012 г. № 1511н).
• СанПин 3.1.5 2826-10 «Профилактика ВИЧ-инфекции».
При постановке ВИЧ-инфицированного пациента на диспансерный учет необходимо ознакомить его с алгоритмом и целью диспансерного наблюдения, графиком посещения лечащего врача и узких специалистов, возможностью выполнения лабораторных и инструментальных исследований. При этом необходимо согласие пациента на проведение диспансерного наблюдения (или отказ от медицинской помощи) в письменном виде.
Мероприятия, проводимые при первичном обследовании
• Осмотр лечащего врача (консультирование, сбор анамнеза, полное физикальное обследование).
• Регистрация вторичных заболеваний, их динамики и течения.
• Регистрация сопутствующих заболеваний.
• Оценка качества жизни пациента (по шкале Карновского).
• Рентгенография органов грудной клетки (если исследование не выполняли в течение последних 6 мес).
• УЗИ органов брюшной полости (печень, желчный пузырь, поджелудочная железа) и почек.
• ЭКГ.
• Консультация офтальмолога (исследуют глазное дно).
• Консультация оториноларинголога (исследуют остроту слуха и состояние вестибулярной функции).
• Консультация невропатолога.
• Консультация стоматолога.
• Консультация гинеколога (для женщин).
• Консультация терапевта.
• Исследование сыворотки или плазмы крови на антитела к ВИЧ с помощью стандартных лабораторных технологий, разрешенных к применению в Российской Федерации.
• Общий анализ крови (гемоглобин и гематокрит, тромбоциты, эритроциты и лейкоциты, лейкоцитарная формула, СОЭ).
• Биохимический анализ крови (креатинин и мочевина, активность АЛТ, АСТ, ЩФ, ЛДГ, КФК, амилазы или липазы, билирубин и его фракции, глюкоза, общий белок и фракции, общий холестерин и его фракции).
• Общий анализ мочи.
• Определения маркеров ВГВ, ВГС.
• Серологический анализ - для обнаружения маркеров сифилиса, антител к ЦМВ, токсоплазме, ВПГ, P. jirovecii.
• Исследование кала на яйца глистов и на простейших; посев для диагностики сальмонеллеза.
• Проба с туберкулином или диаскин-тест с консультацией врача-фтизиатра.
• Определение показателей иммунного статуса.
• ПЦР для определения концентрации РНК ВИЧ в сыворотке крови. Повторные плановые обследования проводят для своевременного выявления показаний к назначению АРТ (или для ее коррекции). Объем планового повторного обследования зависит от стадии болезни и уровня CD4+-лимфоцитов.
Сроки проведения первичных и повторных осмотров осуществляются согласно «Стандарту специализированной медицинской помощи при болезни, вызванной вирусом иммунодефицита человека (ВИЧ-инфекции)», утвержденному приказом Минздрава России от 9 ноября 2012 г. № 758н и «Стандарту первичной медикосанитарной помощи при болезни, вызванной вирусом иммунодефицита человека (ВИЧ-инфекцией)», утвержденному приказом Минздрава России от 24 декабря 2012 г. № 1511н.
Консультации врача-инфекциониста больных ВИЧ-инфекцией, не получающих АРТ, осуществляются 2 раза в год, при проведении АРТ - 4 раза в год; узких специалистов (гинеколог, невролог, оториноларинголог, офтальмолог, терапевт) - при постановке на учет; далее эти специалисты, а также другие узкие специалисты консультируют больных при наличии показаний.
Рентгенографию (или флюорографию) органов грудной клетки и диаскин-тест необходимо выполнять 2 раза в год, УЗИ органов брюшной полости и почек - 1 раз в год или чаще при наличии показаний. Исследование головного мозга с помощью метода КТ или МРТ рекомендуют выполнять по показаниям при резком снижении количества CD4+-лимфоцитов (<200 мкл 1).
Внеплановые обследования необходимо проводить при обнаружении любых признаков прогрессирования ВИЧ-инфекции или при развитии сопутствующих заболеваний. По решению лечащего врача выполняют дополнительные исследования.
Прогноз
Прогноз заболевания, вызванного ВИЧ, в целом неблагоприятный, поскольку препараты, приводящие к полной элиминации вируса, отсутствуют. Внедрение АРТ позволило резко уменьшить число летальных исходов и значительно увеличить продолжительность и качество жизни ВИЧ-инфицированных.
Тактика проведения диагностических и лечебных мероприятий по оказанию медицинской помощи при болезни, вызванной ВИЧ у взрослого населения, представлена в табл. 21.14-21.16.
Таблица 21.14. Тактика проведения лечебно-диагностических мероприятий при первичном обращении ВИЧ-инфицированного за медицинской помощью
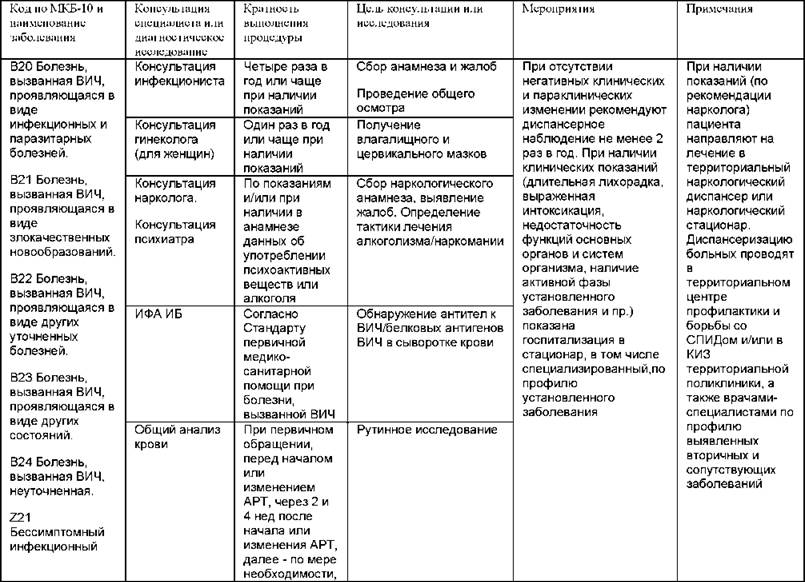
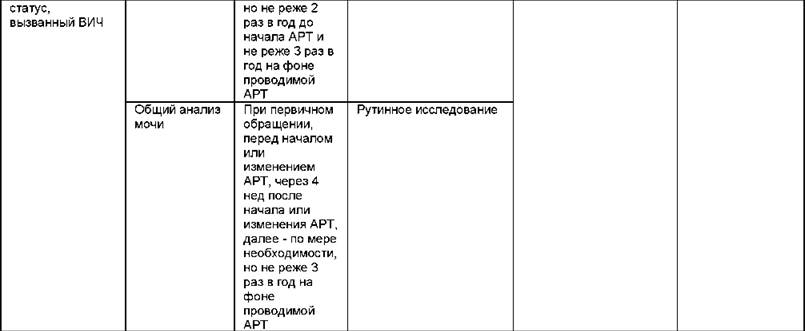
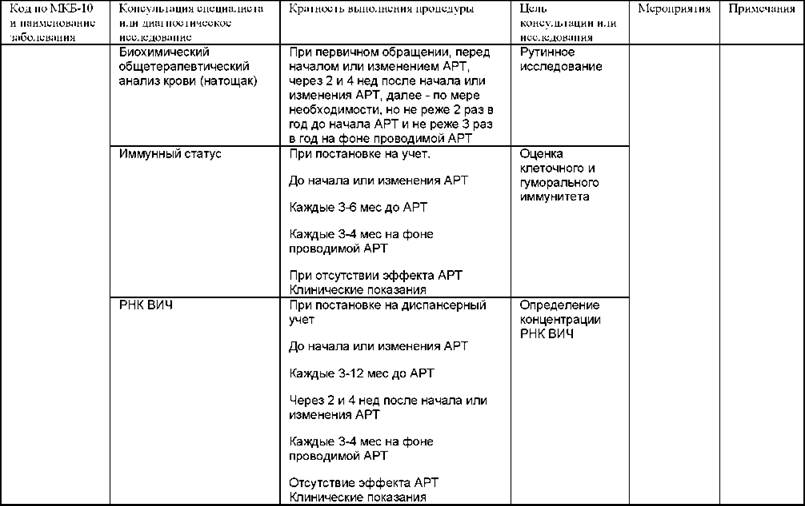
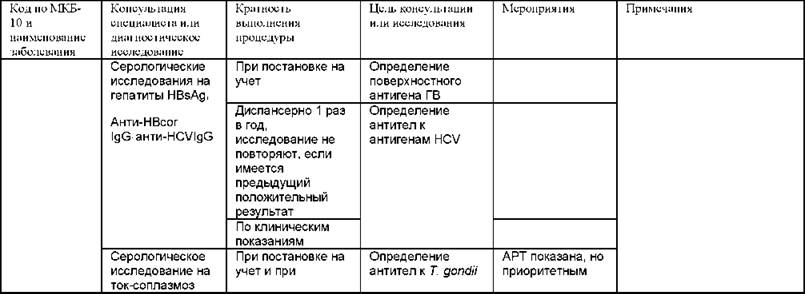
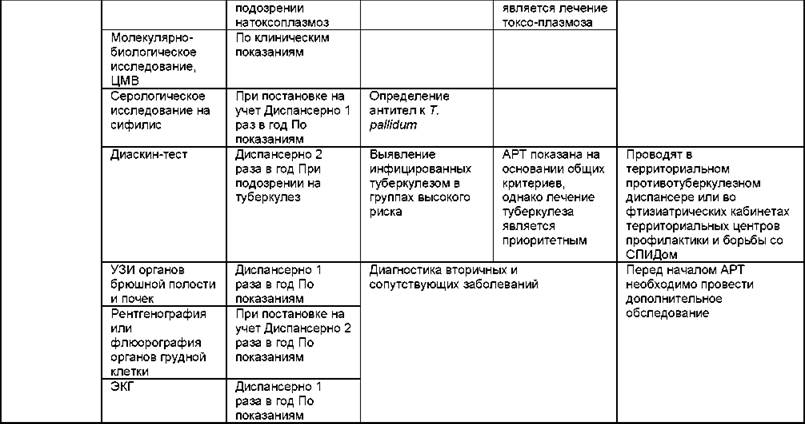
Таблица 21.15. Тактика проведения лечебно-диагностических мероприятий при обращении ВИЧ-инфицированного пациента за медицинской помощью
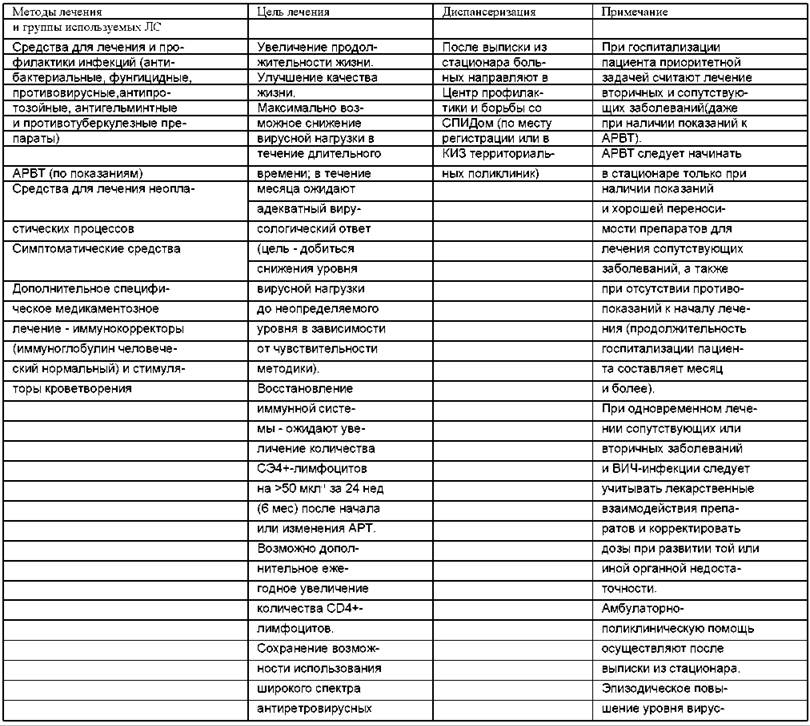
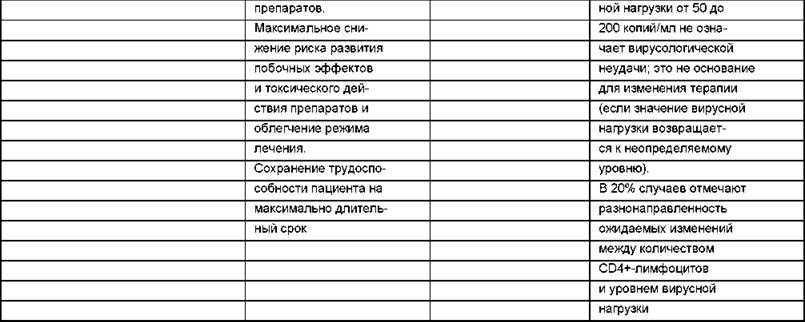
СПИСОК ЛИТЕРАТУРЫ
1. Бартлетт Дж., Редфилд Р., Фам П., Мазус А.И. Клинические аспекты ВИЧ- инфекции. Российское издание 2013. - М.: ГРАНАТ, 2013. - 696 с.
2. Беляков Н.А., Рахманова А.Г. ВИЧ-медицина / Под. ред. Н.А. Белякова, А.Г. Рахмановой. - 3-е изд. - СПб.: Балтийский медицинский образовательный центр, 2012. - 656 с.: ил.
3. Бессараб Т.П., Голохвастова Е.Л., Данилычева И.В. и др. Иммунология. Фармакотерапия без ошибок. Рук. для врачей / Под ред. Р.М. Хаитова. - М.: Е-ното, 2016. - 504 с.
4. Бессараб Т.П. Аспекты ВИЧ-инфекции и СПИД в оториноларингологии // Вестник оториноларингологии. - М., 2004. - № 1. - C. 15-23.
5. Бобкова М.Р. Лекарственная устойчивость ВИЧ. - М.: Человек, 2014. - 288 с.
6. Володин Н.Н., Адамян Л.В., Курцер М.А. и др. Проведение профилактики передачи ВИЧ-инфекции от матери ребенку. Клинические рекомендации. - М.: РАСПМ, 2015. - 34 с.
Таблица 21.16. Дополнительные методы обследования ВИЧ-инфицированных пациентов
|
Дополнительные медицинские |
манипуляции |
Кратность выполнения и причина |
|
Лабораторная диагностика |
Коагулограмма Определение маркеров прочих ВГ Посев крови на стерильность Посев мокроты на флору Посевы биологических сред на флору и определение чувствительности к антибиотикам Микроскопия мокроты (с окраской по Граму и Цилю- Нильсену) Определение ДНК ЦМВ методом ПЦР |
По клиническим показаниям |
|
И нструментальная диагностика |
УЗИ органов малого таза, ЛУ, крупных сосудов, сердца КТ, МРТ, ПЭТ КТ ЭГДС Биопсия ЛУ, печени и других органов Фибробронхоскопия Спинномозговая пункция |
По клиническим показаниям |
|
Процедуры, выполняемые перед назначением АРВТ |
Консультации невролога, офтальмолога, оториноларинголога, нарколога, терапевта, при необходимости эндокринолога, нефролога и гематолога |
При первичном обращении пациента, затем по клиническим показаниям |
|
Определение уровня лактата в сыворотке крови |
Только при наличии симптомов лактатацидоза |
|
|
Определение натощак общего уровня холестерина, липопротеинов высокой и низкой плотности, триглицеридов, содержания глюкозы крови (натощак) |
При первичном обращении пациента, затем каждые 3-6 мес на фоне АРВТ и по клиническим показаниям |
|
|
Резистентность к препаратам (генотипирование) |
До начала или изменения АРВТ и по показаниям |
7. Либман Г., Макадон Х. Дж. ВИЧ-инфекция / Пер. с англ. под ред. А.И. Мазуса, Т.П. Бессараба - М.: ГЭОТАР-Медиа, 2012. - 560 с.: ил.
8. Лысенко А.Я., Турьянов М.Х., Лавдовская М.В., Подольский В.М. ВИЧ-инфекция и СПИД-ассоциируемые заболевания. - М.: ТОО «Рарогъ», 1996. - 624 с.
9. Мазус А.И., Влацкая Ю.Ф., Бессараб Т.П. и др. Национальные клинические рекомендации по диагностике и лечению ВИЧ-инфекции у детей и подростков. - М.: НВА, 2014 г. - 18 с.
10. Мазус А.И., Голиусов А.А., Мартынов Ю.В. и др. ВИЧ-инфекция: динамика эпидемического процесса // РМЖ. - 2006. - № 4. - С. 3-7.
11. Мазус А.И., Каминский Г.Д., Бессараб Т.П. и др. Национальные клинические рекомендации по диагностике и лечению ВИЧ-инфекции у взрослых. - М.: НВА, 2013. - 69 с.
12. Пархоменко Ю.Г., Зюзя Ю.Р., Мазус А.И. Морфологические аспекты ВИЧ- инфекции - М.: Литтерра, 2016. - 168 с.: ил.
13. Рокштро Ю.К., Хоффман К. Лечение ВИЧ-инфекции «ВИЧ 2014/2015». - Hamburg, Medizin Fokus Verlag, 2015. - 924 с. - www.hivbuch.de
14. Сааг М., Чемберс Г., Элиопулос Дж. И др. Лечение ВИЧ-инфекции и вирусных гепатитов по Дж. Сэнфорду / Пер. с англ. под ред. А.И. Мазуса, Т.П. Бессараба - М.: ГРАНАТ, 2015. - 632 с.
15. Ющук Н.Д., Венгеров Ю.Я. Лекции по инфекционным болезням. - 4-е изд., перераб. и доп. - М.: ГЭОТАР-Медиа, 2016. - 1248 с.
16. Guidelines for the Use of Antiretroviral Agents in HIV-1-Infected Adults and Adolescents, DHHS, 2016. http://aidsinfo.nih.gov/guidelines
17. Recommendations for Use of Antiretroviral Drugs in Pregnant HIV-1-Infected Women for Maternal Health and Interventions to Reduce Perinatal HIV Transmission in the United States. - 2016. http://aidsinfo.nih.gov/guidelines/html/3/perinatal-guidelines/0
18. European Guidelines for treatment of HIV-infected adults in Europe. - 2016. http:// europeanaidsclinicalsociety.org/